
软性电活性水凝胶具有生理力学模量小、电阻低、对生物组织电生理信号具有双向刺激和记录能力等优点,是构建组织样假体材料的最佳选择。然而,到目前为止,用于这种假体的生物电子装置一直是补片式的,不能应用于粗糙、狭窄或深层组织表面。在这里,我们提出了一个注射组织假体与瞬间双向电传导性在神经肌肉系统。该软性注射假体由具有苯硼酸盐介导的多重交联的生物相容性水凝胶组成,如不可逆但可自由重排的联苯键和可逆的配位键与原位交叉偶联形成的导电纳米金粒子。在大鼠严重肌肉损伤的早期成功地实现了闭环机器人辅助康复,在后期实现了加速组织修复。
闭环步态康复与轻型外骨骼和可穿戴或可植入装置相结合的进展已经大大改善了患者医疗保健的质量,因为从严重损伤的神经和肌肉系统相关的运动和感觉功能障碍的有效恢复中产生的临床有效性的潜力。尽管取得了这样的进展,实现运动的早期恢复仍然具有挑战性。在这方面,将用于快速组织修复的导电水凝胶策略应用于传统的软组织假体方法,可以解决由于水凝胶的低阻抗、机械模量匹配、组织粘附甚至可生物降解性而未能满足的需求。这种水凝胶满足康复早期电生理组织传导的基本要求,对器官表面进行有效的低阈值电刺激以加速组织再生,并记录闭环保健系统的低噪声生理信号,从而能够进行精确诊断和反馈治疗。
到目前为止,大多数用于神经假体的组织接口生物电子学都是基于贴片型形成因子的,并且在受损组织区域中访问狭窄,复杂和微小的生物界面的能力有限m。另一方面,注射器注射和导电水凝胶近年来取得了进展,可以有效地引入到组织工程和软生物电子学领域的难以进入的场所。然而,大多数具有动态可逆键(例如,宿主-客体相互作用,氢键)的可注射和/或导电材料仅具有嵌入式导电添加剂,由于其弱的分子键和不良凝胶的非均匀电渗透,因此显示出较低的机械和电耐久性,从而不希望阻碍长期稳定的现场组织界面。虽然可以引入强烈的不可逆共价键来提高现有水凝胶的机械性能,但它们常常与这些材料的可注射性相抵消。

近日,韩国成均馆大学Mikyung Shin教授、韩国基础科学研究所Donghee Son教授合作报道了一种广泛应用的皱纹除皱填充材料透明质酸。利用这种物质,研发了一种可注射的“组织仿生水凝胶”,该水凝胶可以在肌肉和神经组织再生的同时,临时填充缺失的肌肉和神经组织空隙。相对于传统的生物电子装置,这种材料的可注射性带来了显著的优势,因为传统的生物电子装置不适合用于狭窄、深层或小面积区域,并且通常需要侵入性手术。由于其高度类似生物组织的特性,这种水凝胶能够与生物组织无缝接触,无需手术干预即可轻松应用于难以触及的身体部位。相关研究以“ Injectable tissue prosthesis for instantaneous closed-loop rehabilitation”为题发表在 Nature 上。
在本文研究中,导电水凝胶(IT-IC)的聚合物骨架是由透明质酸构成的。透明质酸是一种天然存在的多糖,具有与软组织相似的机械性能。IT-IC水凝胶包含不可逆的联苯键,可逆的强配位键,以及由联苯偶联和PB基团原位还原的导电金纳米颗粒(AuNPs)之间的强配位键,还包括氢键、金属π键和金属羧酸盐在多糖骨架上的相互作用。PB衍生的多键通过弱非共价键的解离以及在注射过程中的剪切应力下的联苯重排,共同实现了有效的能量耗散。因此,这种材料允许从肌肉产生的电信号通过机器人康复系统进行辅助传递。该康复系统具备能够进行周围神经刺激和监测反馈肌电图(EMG)的闭环系统,以实现精确的控制。
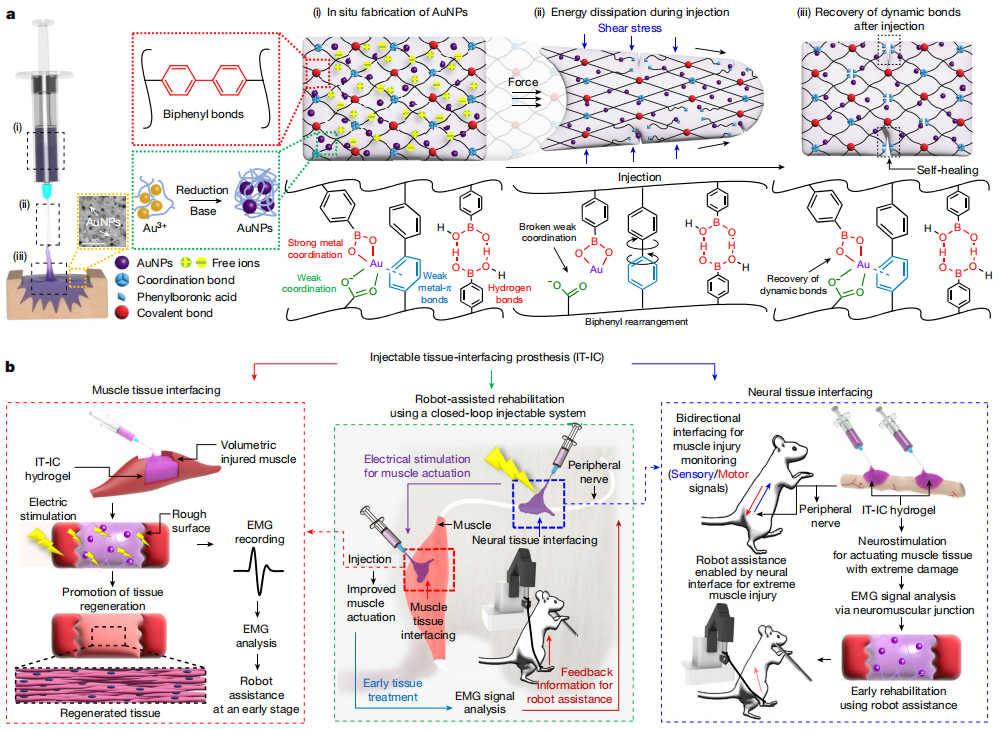
图1. 可注射组织假体(IT-IC 水凝胶)的设计及其界面应用
当水凝胶应用于经常遭受拉伤的组织(如骨骼肌)时,水凝胶的结构弱点成为一个重要问题。简单地在透明质酸骨架上引入更多不可逆的共价键并不是解决之道,因为这会使水凝胶过于坚硬而无法流动。在这项研究中,作者引入了可逆键,比如由六边形环提供的键,或通过氢键和离子相互作用形成的键,它们在凝胶被推入针头时能够在受到“剪切力”作用下破裂。这使得水凝胶在注射时可以轻松流动,但也意味着一旦水凝胶在受伤的肌肉中固化,可以快速重新建立键,从而实现长期的稳定性。
水凝胶内的可逆和不可逆交联相结合,适应了注射过程中的高剪切应力,确保了出色的机械稳定性。这种水凝胶还添加了金纳米颗粒,使其具有出色的电导性能。这种导电性能使电生理信号能够在受伤组织的两端之间有效传输。此外,水凝胶是可生物降解的,这意味着患者不需要再次接受手术来移除它。由于具有类似于天然组织的机械性能、出色的组织附着性和可注射性,研究人员认为这种材料提供了一种全新的康复方法。
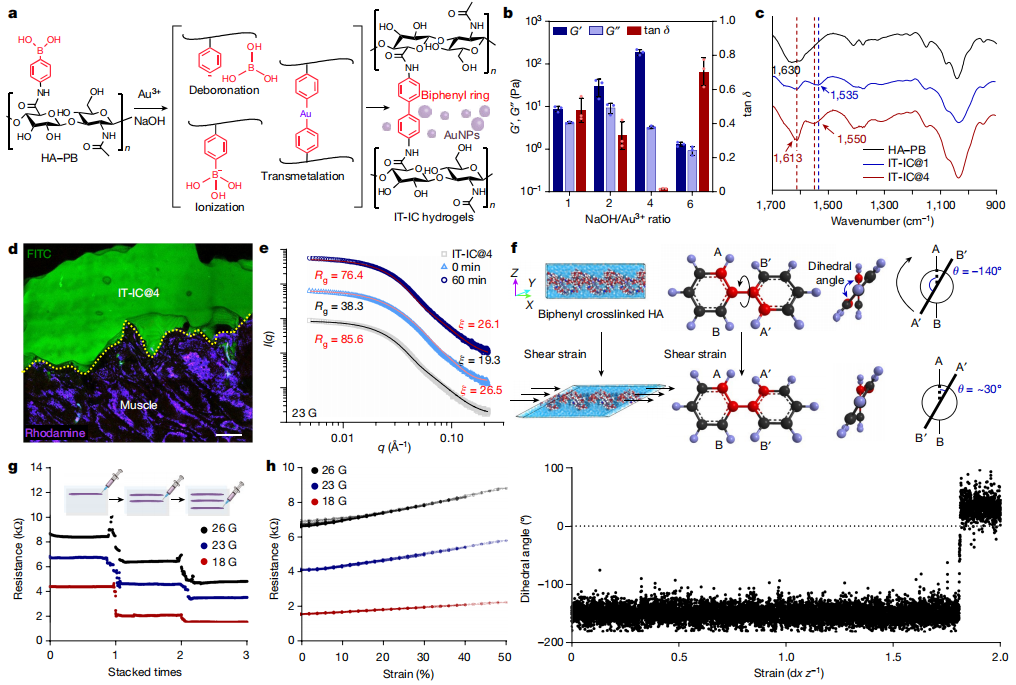
图2. IT-IC 水凝胶的物理化学和电学特性分析
随后,研究人员在啮齿动物模型中对这一新的概念进行了测试。为了模拟大体积肌肉损伤,他们从这些动物的后腿上移除了一大块肌肉组织。通过注射水凝胶假体,能够支持大鼠后腿受伤骨骼肌的再生,水凝胶假体在四周内几乎完全降解。重要的是,假体不会导致大鼠免疫系统的过度激活,也不会形成疤痕状纤维组织。
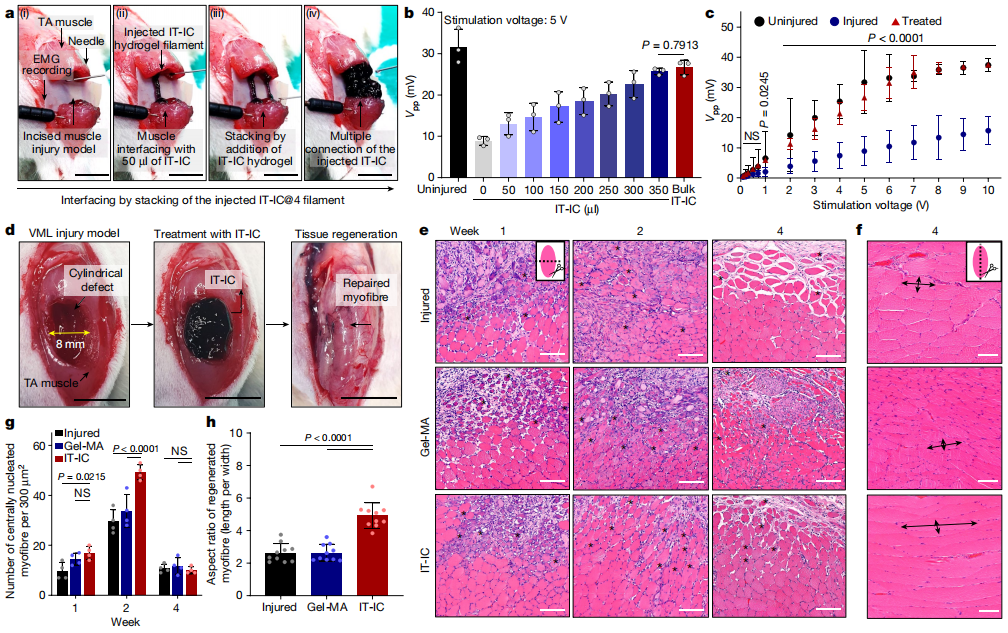
图3. 通过注射 IT-IC 水凝胶制作骨骼肌组织假体
与传统薄膜型生物电贴片的器官附着方法相比,他们的 IT-IC 水凝胶具有可注射性,因此能够与因外科手术、创伤性损伤、先天性或后天性畸形等各种事件而受伤的狭窄和/或深层难以触及的组织无缝对接。在进行以下生物测试之前,他们对 IT-IC@4 的体外解离情况进行了研究,结果表明 IT-IC@4 在生理条件下会溶胀 2 天,并在 5 天内缓慢解离,释放出 AuNPs。作为一种组织界面材料,IT-IC 水凝胶的生物相容性足以使两种不同的神经元样细胞(已分化的 PC12 和 HT22 细胞)在水凝胶释放物的处理下保持约 99% 的存活率。此外,他们还证实了 IT-IC 水凝胶的离体导电能力。电信号成功地从一块受刺激的肌肉通过 IT-IC 传输到另一块待记录的肌肉,与其他对照组相比,IT-IC@4 接口的肌电图振幅(2.2 mV)最高。为了更好地阐明 IT-IC 水凝胶在体内组织间传导的能力,他们将 IT-IC 水凝胶应用于通过对整个组织进行横截面切割而建立的肌肉损伤模型,这种切割会导致受损组织表面复杂粗糙,而且损伤不可恢复,有可能干扰精确的预期运动识别,而这正是进行早期闭环机器人辅助康复(C-RAR)的关键要求。
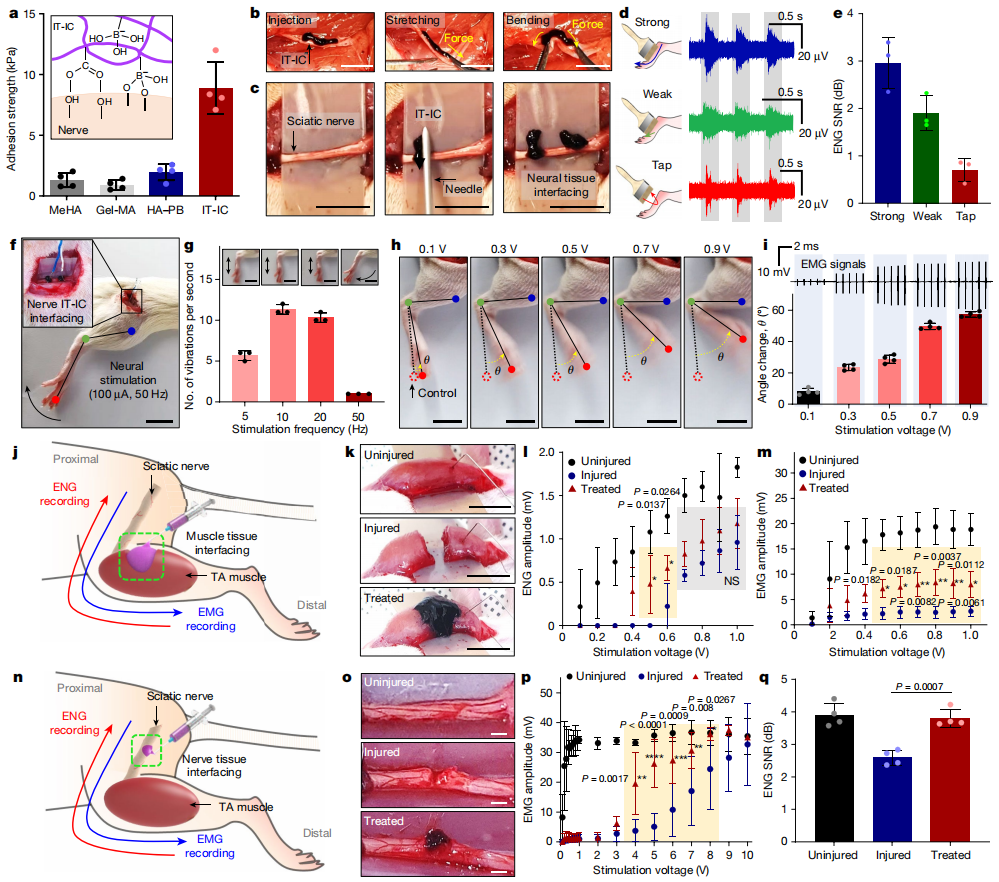
图4. 神经肌肉系统中 IT-IC 水凝胶的双向感觉和运动信号传递
研究团队一直在努力开发具有有效电荷传输和组织再生能力的 IT-IC 水凝胶,并将其应用于麻醉大鼠体内双向感觉和运动信号传导,在此基础上,进一步将 IT-IC 水凝胶应用于 C-RAR,使肌肉损伤的苏醒大鼠在早期阶段就能活动。
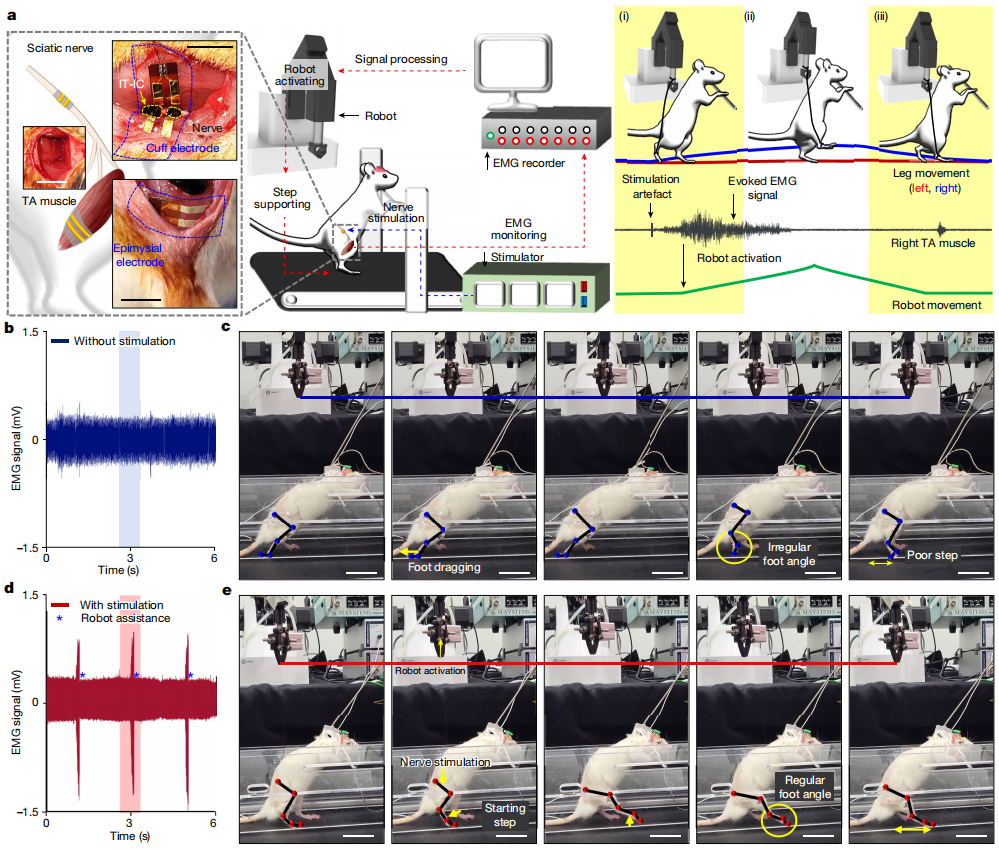
图5. 使用 IT-IC 水凝胶的 C-RAR 系统
综上,由柔软且可传导的透明质酸水凝胶组成的可注射假体可在损伤后的早期阶段通过肌肉和周围神经组织传导实现瞬时 C-RAR,并在后期阶段加强组织修复。在水凝胶网络中,由可重新排列的联苯键辅助的动态配位键在确保与组织相似的理想机械模量、通过对剪切应力的有效能量消耗实现的高注射性、粗糙组织界面上的保形接触以及抗应变导电性方面发挥着关键作用。将 IT-IC 水凝胶应用于组织缺陷和设备-组织界面可实现电生理信号的传输和监测。最终,可注射假体平台可在肌肉和周围神经组织之间实现双向串扰,促进慢性组织损伤患者的治疗康复。
以上文章转载于微信公众号化学与材料科学,如有侵权,请及时联系我们修改或进行删除。