
在电子器件领域,实现柔软的生物组织与硬质电子设备的标准化接口一直是一项挑战。生物组织不仅柔软,其形状和尺寸也多种多样。如果能开发出一种生物相容性薄膜,类似于工业包装中常见的“热收缩膜”,或许能够实现对各种形状和尺寸的生物-电子接口的理想匹配。然而,寻找能制造这种生物相容性收缩薄膜的材料并非易事。常见的热收缩膜往往比生物组织更硬,而且需要较高温度才能收缩,无法在人体温度下使用。在体温和水刺激下收缩的材料与生理环境更相容,但又往往收缩太过缓慢或稳定性不佳。水凝胶足够柔软,可以最大限度地减少与生物组织的机械不匹配,但它们的高含水量使它们与普通的微电子制造工艺不相容。
蜘蛛丝被认为是最坚韧的天然材料之一,兼具机械强度和延展性的优点。更独特的是,在高湿度环境下,蜘蛛牵引丝(dragline)的长度会急剧收缩约60%,该过程通常被称为超收缩现象,其机理归因于牵引丝独特的分层结构,以及高相对湿度触发微观结构的转变。
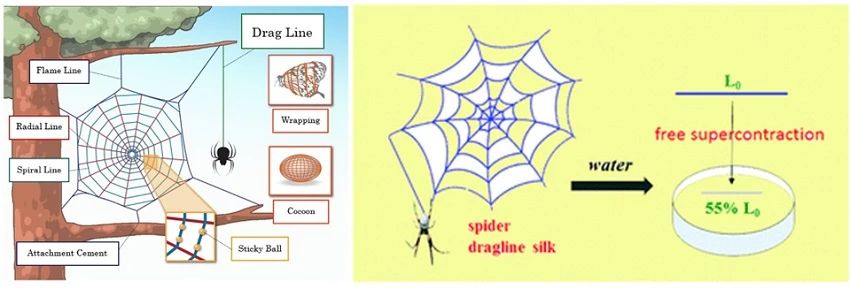
蜘蛛牵引丝及超收缩现象。图片来源:Molecules [1] & J. Mater. Chem. B [2]
受到蜘蛛牵引丝遇水超收缩现象的启发,近日南洋理工大学陈晓东院士和高华健院士、中国科学院深圳先进技术研究院刘志远研究员、南京医科大学胡本慧教授等研究者合作,开发出一种新型水响应超收缩聚合物薄膜,解决了生物组织与电子器件界面的无缝连接问题,为实现生物和电子设备之间的标准化集成提供了新的可能性。
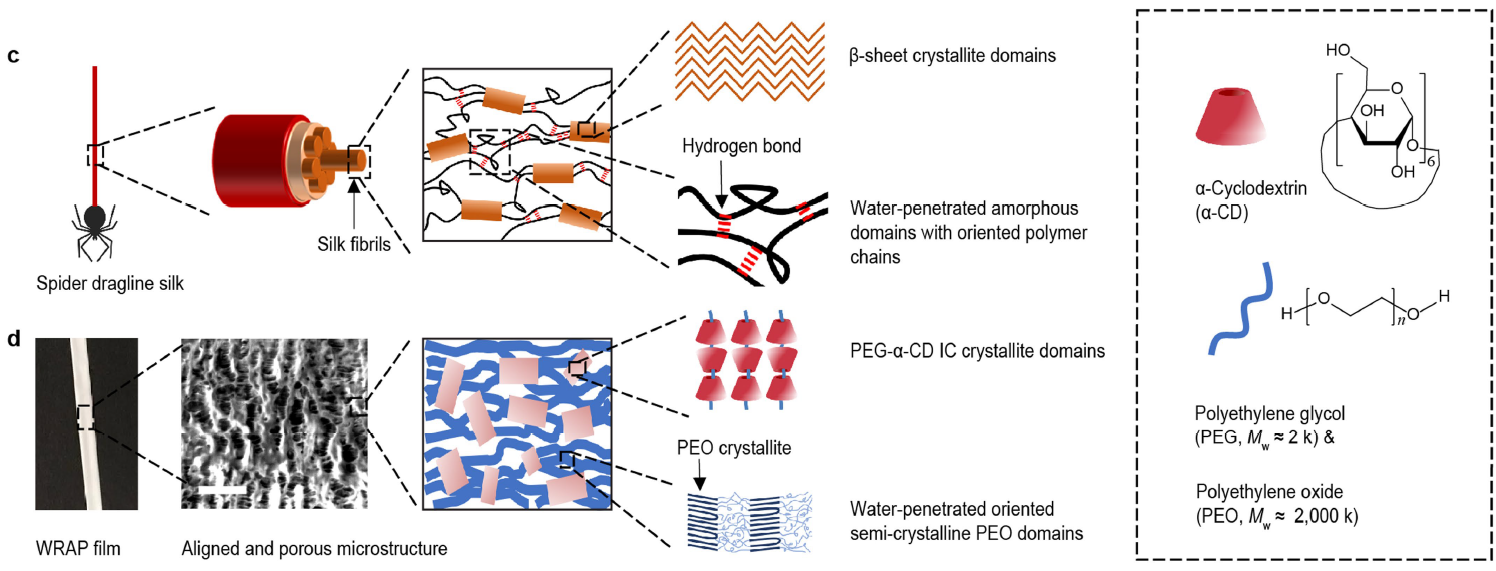
受蜘蛛牵引丝启发的水响应超收缩聚合物薄膜。图片来源:Nature
研究者将半晶态聚氧化乙烯(PEO)颗粒溶解在水中,与聚乙二醇-α-环糊精凝胶混合并进行交联,经过溶剂铸膜、干燥和反复冷拔就得到了水响应形状可塑聚合物薄膜(WRAP)。自然环境下,薄膜的可拉伸范围从218%到700%,将其浸泡在水中后,薄膜会迅速收缩,变成柔软且可拉伸的水凝胶薄膜,对应的收缩比从35%到65%,其杨氏模量也下降了三个数量级以上。而且,当相对湿度低于80%时,薄膜并不会发生收缩,这表明它们在普通环境湿度下具有稳定性。
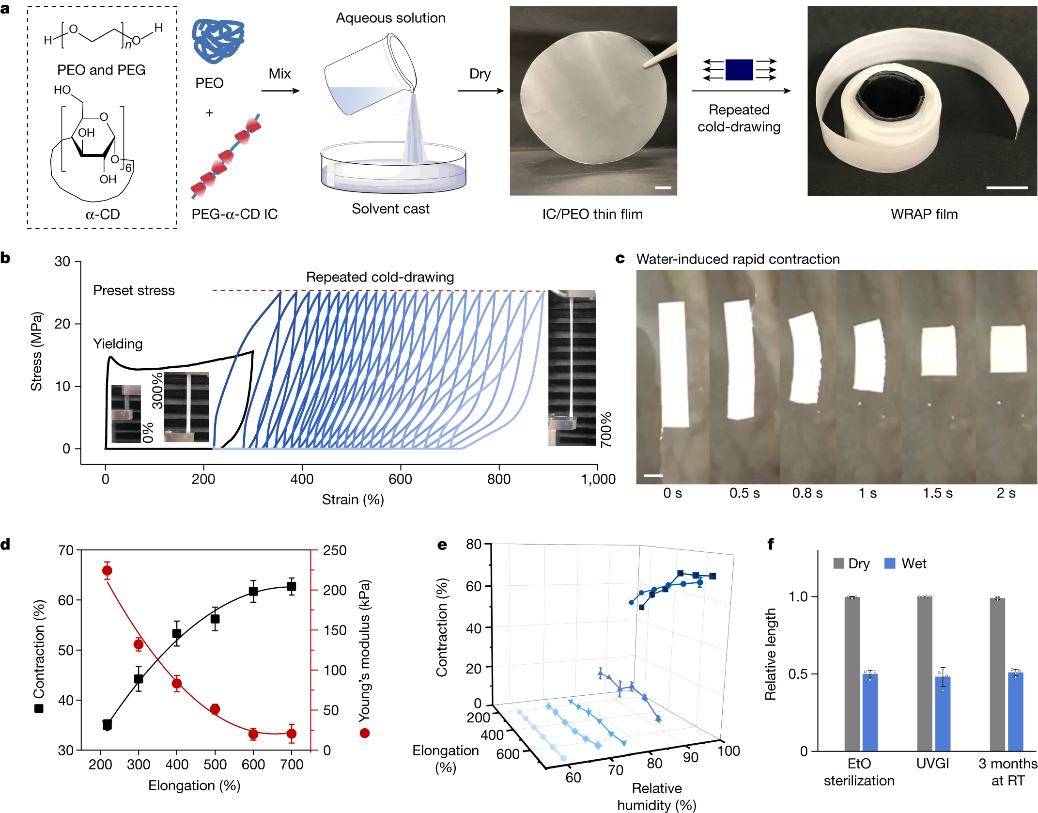
水响应形状可塑聚合物薄膜。图片来源:Nature

WRAP薄膜遇水超收缩。图片来源:Nature
薄膜的超收缩性能与微观结构密切相关。测试显示,薄膜在冷拔时产生多孔微结构,并使PEO微晶和链发生取向,暂时被PEO再结晶域固定。将薄膜放入水中后,PEO结晶域被水破坏和溶解,引起了薄膜的超收缩。而聚乙二醇-α-环糊精凝胶部分则保证了多孔微结构的形成,以及遇水收缩后薄膜的稳定性。
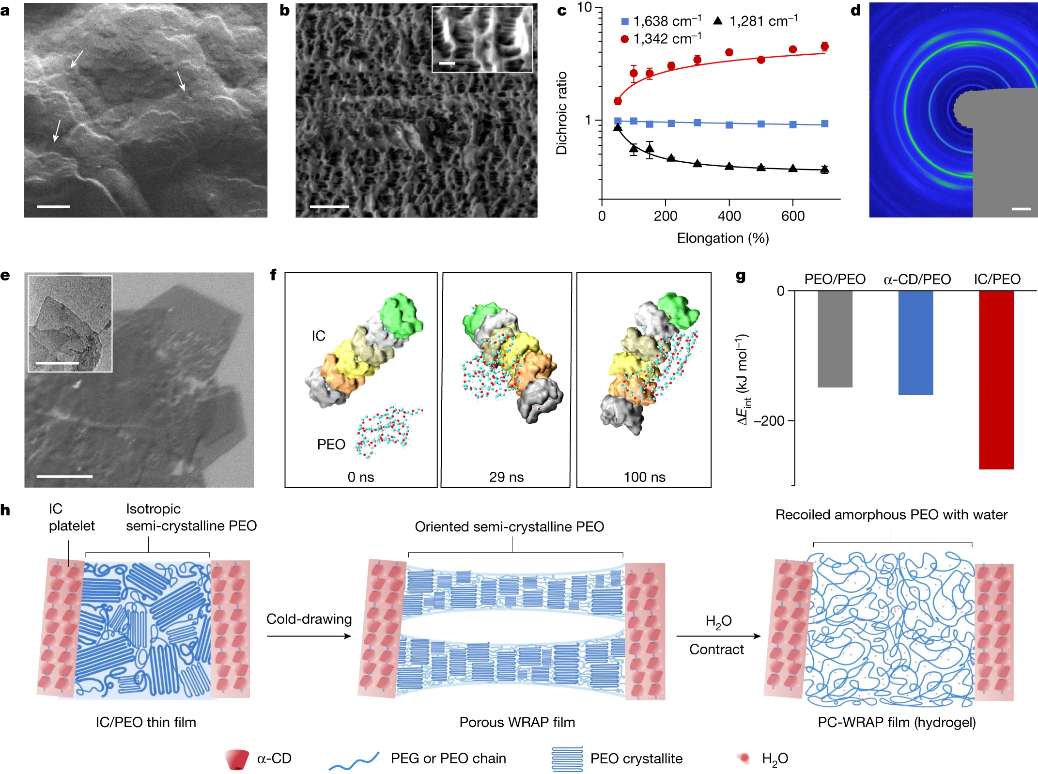
WRAP薄膜的微观结构和超收缩机理。图片来源:Nature
随后,研究者通过真空蒸镀和旋涂法在WRAP薄膜上分别沉积了金(Au)和嵌段共聚物SEBS,得到的WRAP-Au薄膜同样表现出良好的柔性。在湿润条件下,WRAP-Au薄膜发生收缩,其阻抗和相位角值在20%和40%应变时几乎保持不变。体外测试结果显示,经过循环拉伸和在生理盐水中浸泡2周后,WRAP-Au电极依旧具有稳定的性能。
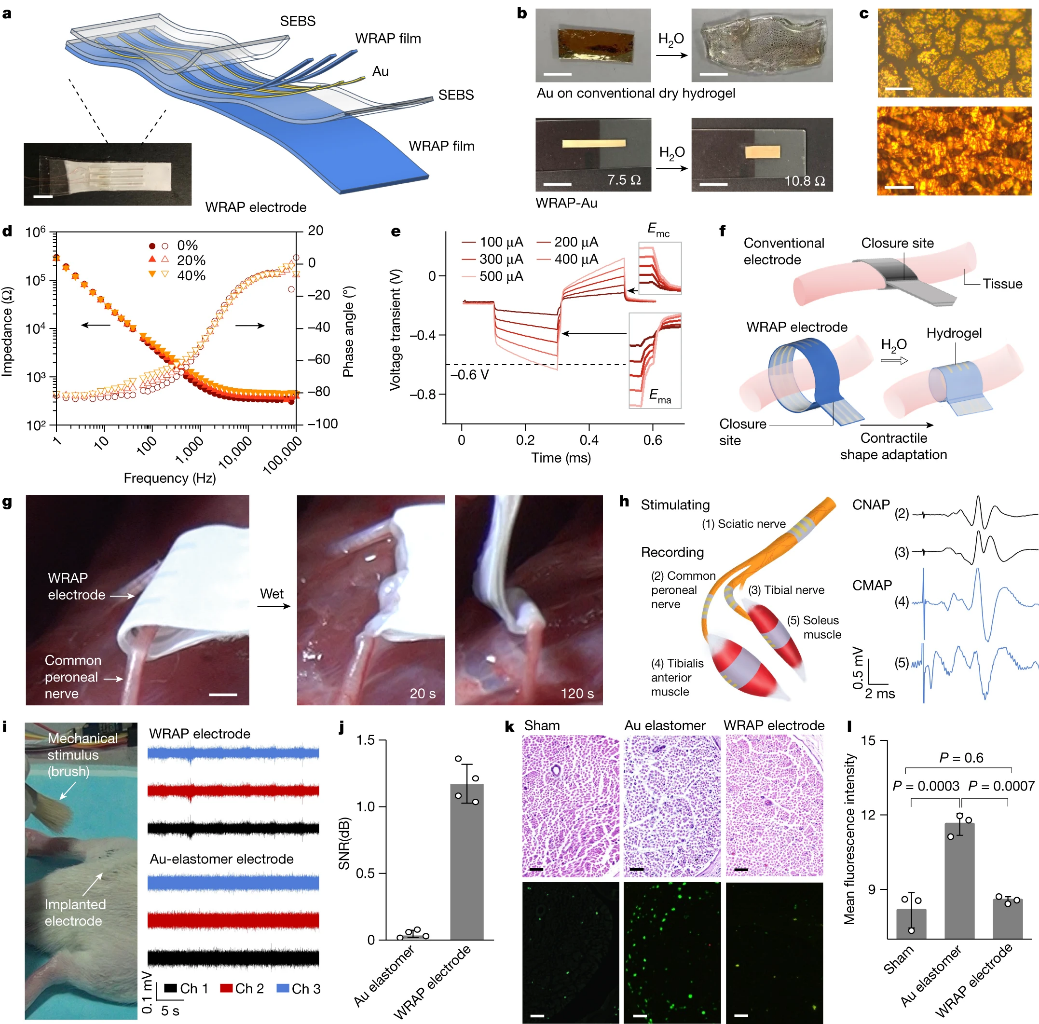
WRAP-Au电极制备及应用。图片来源:Nature
利用WRAP-Au电极的水响应超收缩以及形状自适应,可以轻松植入生物组织,并用于电生理信号记录或神经刺激。在植入组织时,可以事先在组织较远处放置电极,因此减小了组织损伤的风险。研究者在大鼠坐骨神经和较小的胫骨神经等处预置了WRAP-Au电极。尽管神经大小不同,但在浸湿后,电极都会收缩成适应形状的薄膜,包裹在神经周围,并应用于神经脉冲刺激以及记录神经动作电位和神经电图(ENG)。
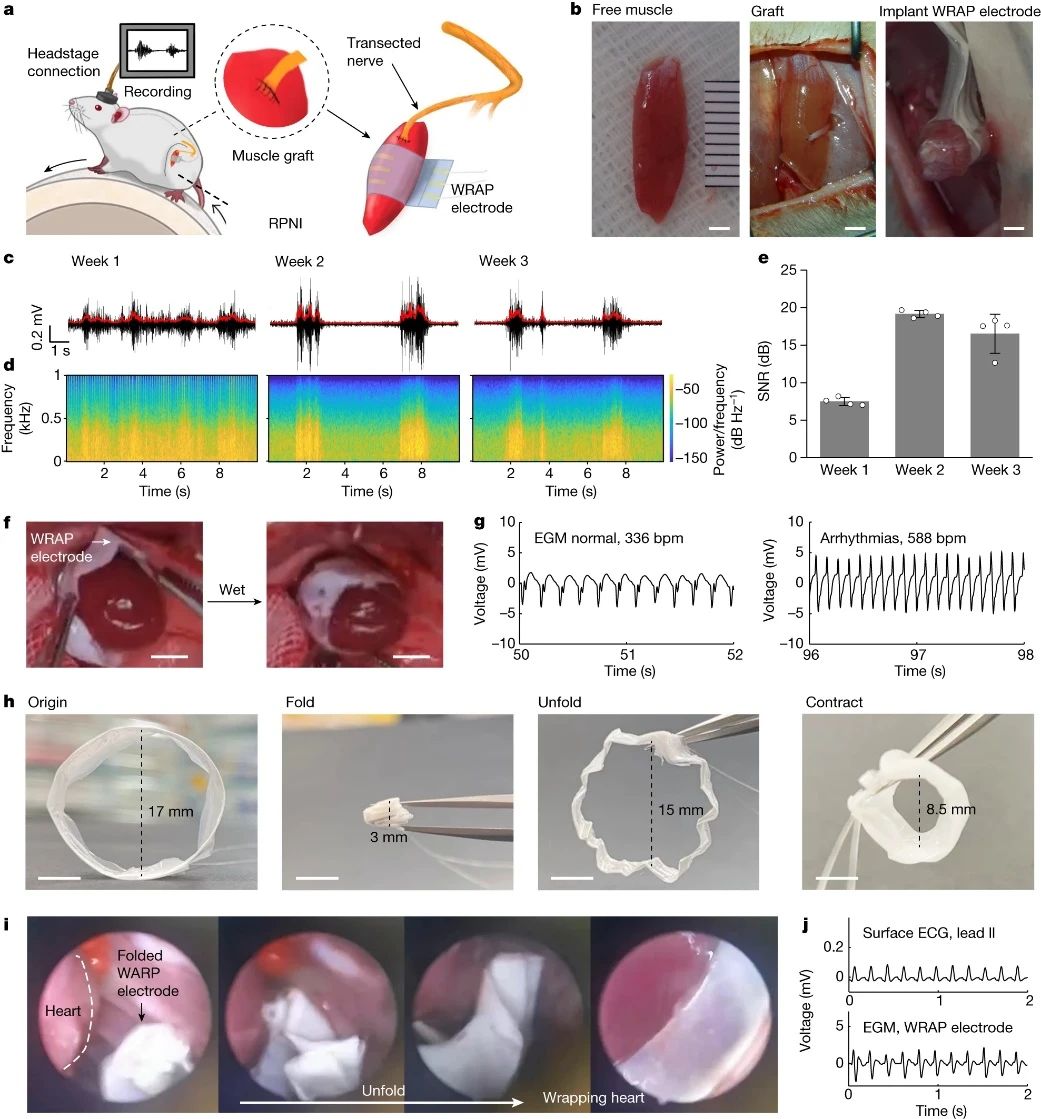
WRAP-Au电极微创植入及应用。图片来源:Nature
研究者进一步将WRAP-Au电极包裹在大鼠的肌肉上,记录了肌电图信号(EMG)。由于薄膜收缩后具有自适应性,可以紧贴在大小和形状都不规则的肌肉表面,使得振幅、信噪比等均表现良好。类似地,WRAP-Au电极还可以包裹在大鼠的心脏周围,并记录大鼠心脏的心电图。
“报道的材料与水接触时的收缩反应对生物医学领域非常有吸引力,尤其是植入手术。这是我读过的关于柔性材料的最令人印象深刻的论文之一”,约翰霍普金斯大学医学院Nitish Thakor评论道。Nature 杂志的首席编辑Karl Ziemelis也认为,“精密的生物组织可以有效地和电子元件一起被‘收缩包裹’,促进了各种传感和神经刺激应用”。研究者则表示,下一个挑战或许是进一步改进交联PEO,得到更稳定的薄膜。[3]
以上文章转载于微信公众号X-MOL资讯,如有侵权,请及时联系我们修改或进行删除。